يشير تآكل المعادن إلى تدهور المواد الناجم عن التفاعل بين المعدن وبيئته. وهي عملية كهروكيميائية، حيث تؤدي أي حالة تسهل تدفق الإلكترونات إلى تسريع التآكل.
1- أنواع تآكل المعادن
واعتمادًا على بيئة التآكل ونوع المعدن، يمكن تصنيف التآكل إلى ثلاثة أشكال: تغير اللون والتآكل والصدأ.
- تغير اللون
تغير اللون هو شكل خفيف من أشكال التآكل السطحي الذي يؤدي إلى تغيرات في اللون أو فقدان البريق. وهو لا يؤثر بشكل عام على السلامة الهيكلية للمعدن بل على مظهره فقط. يمكن للمعادن مثل النحاس والفضة أن يتغير لونها في البيئات التي تحتوي على الأكسجين أو الكبريت أو الهالوجينات، مكونة أكاسيد أو كبريتيدات، خاصةً في الظروف الرطبة.
- التآكل
ينطوي التآكل على أضرار أكثر شمولاً وتغيرات في الخواص المعدنية. على سبيل المثال، عندما يتآكل الألومنيوم أو الزنك، فإنه يشكل مسحوقاً أبيض، ويشكل النحاس طبقة خضراء.
- الصدأ
الصدأ هو تآكل المعادن الحديدية مثل الحديد، مما يؤدي إلى تكوين أكاسيد الحديد، وهو أكثر أنواع التآكل شيوعًا.
2- آلية التآكل المعدني الشائع
يتمثل جوهر التآكل في تبادل الإلكترونات بين سطح المعدن وبيئته. في هذه العملية، يتأكسد المعدن، مما يؤدي إلى تفاعلات كهروكيميائية. على سبيل المثال، في تآكل الحديد مع قطرات الماء، تتشكل خلية تركيز، مما يسبب التآكل. يكون محتوى الأكسجين في مركز قطرة الماء أقل من محتوى الأكسجين في الأطراف، مما يؤدي إلى تكوين منطقة أنود وكاثود، مما يؤدي إلى تكوين الصدأ.
آلية تكوّن الصدأ على سطح الحديد
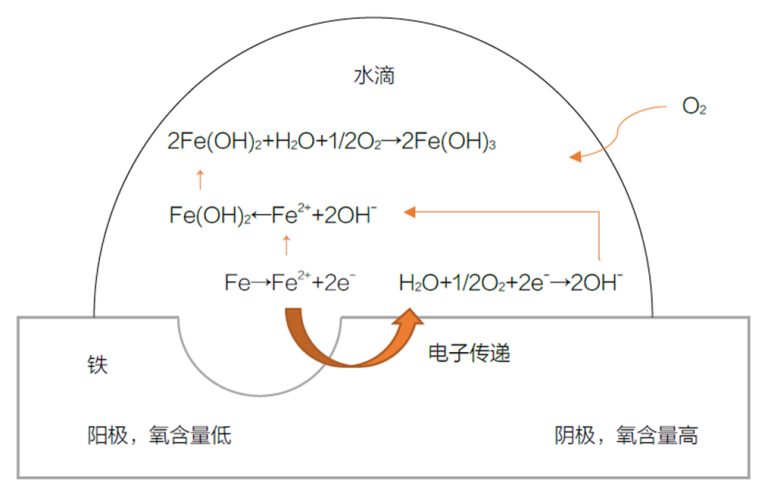
- تعمل منطقة الأكسجين المنخفضة كمصعد، حيث تفقد ذرات الحديد الإلكترونات وتصبح أيونات حديد: الحديد ⁺ Fe → Fe²+2e-
- عند حافة قطرة الماء، يختزل الماء والإلكترونات المنطلقة الأكسجين، مكوِّنين أيونات الهيدروكسيد (منطقة المهبط): ½ O₂ + H₂O + 2e- → 2OH-
- تتحد أيونات الهيدروكسيد مع أيونات الحديد لتكوين هيدروكسيد الحديدوز: Fe²⁺ + 2OH- → Fe(OH)₂
- يتفاعل هيدروكسيد الحديدوز كذلك مع الماء والأكسجين، مكونًا الصدأ البني: 2Fe(OH)₂+ H₂O + ½ O₂ → 2Fe(OH)₃
3- أنواع التآكل
3.1 التآكل المنتظم 3.1 التآكل المنتظم
عندما يغطي الماء أو السوائل الأخرى سطح المعدن بالكامل، تتغير مناطق الأنود والكاثود باستمرار، مما يؤدي إلى تآكل منتظم. وهذا هو الشكل الأكثر شيوعًا للتآكل المعدني اليومي.
3.2 تأثيرات الإلكتروليت
تتميز المياه النقية بقدرة منخفضة على التآكل بسبب قدرتها المنخفضة على التأين. ومع ذلك، فإن إضافة الأحماض أو القواعد أو الأملاح تزيد من تركيز الأيونات، مما يسرّع التآكل. وفي بعض الحالات، تتفاعل الإلكتروليتات مع سطح المعدن لتكوين طبقة تخميل تبطئ عملية التآكل.
3.3 تآكل تركيز الأكسجين
كما هو موضح سابقًا، تعمل منطقة الأكسجين المنخفضة كأنبوب، وتعمل منطقة الأكسجين المرتفعة كمهبط، مما يسبب تآكل خلية تركيز الأكسجين.
3.4 التآكل الجلفاني
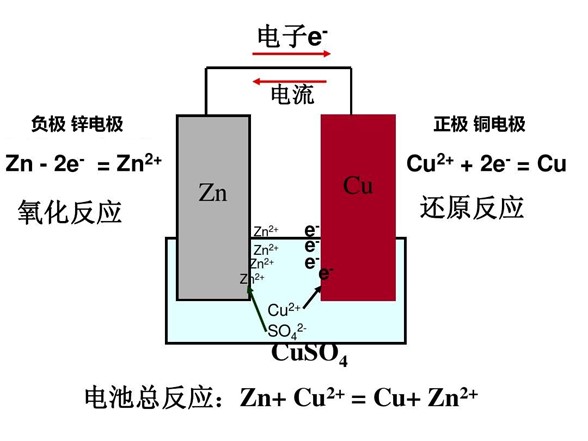
عندما يتم غمر معادن مختلفة في نفس السائل، يحدث تفاعل كهروكيميائي، مما يسبب التآكل الجلفاني. وهذا هو المبدأ الذي تقوم عليه البطاريات.
مبدأ البطارية
3.5 تآكل التآكل
يحدث تآكل التآكل عندما تقوم السوائل سريعة التدفق بإزالة السطح المعدني ميكانيكيًا. وهذا مهم بشكل خاص في خطوط الأنابيب وأنظمة المضخات.
3.6 تآكل التآكل
وعلى غرار التآكل، يحدث التآكل المتآكل عندما تزيل المواد الصلبة الأغشية الواقية من الأسطح المعدنية، وهو ما يظهر عادةً في نقاط التلامس بين الأجزاء.
3.7 التآكل بالتأليب
ويحدث التآكل النقر عندما تتعرض مناطق صغيرة من سطح المعدن للتآكل الموضعي. على سبيل المثال، عندما تتعرض طبقة الأكسيد الواقية للخدش، تصبح المنطقة المكشوفة أنودًا، مما يؤدي إلى حدوث حفرة تآكل.
3.8 التآكل بين الخلايا الحبيبية
التآكل بين الخلايا الحبيبية هو نوع من التآكل الموضعي الذي ينتشر على طول حدود حبيبات المعادن. ويحدث في الفولاذ المقاوم للصدأ عند تسخينه لدرجات حرارة معينة، مما يؤدي إلى خلق مناطق مستنفدة من الكروم عند حدود الحبيبات مما يؤدي إلى فقدان مقاومة التآكل.
3.9 تآكل الإجهاد
يحدث التآكل الإجهادي تحت إجهاد الشد، خاصةً في قطع العمل الملحومة ذات الإجهاد المتبقي. يتلف الغشاء الواقي على السطح المعدني، مما يؤدي إلى حدوث تشققات تنتشر بمرور الوقت، مسببة كسورًا.
3.10 التآكل المستحث بالميكروبات
يمكن أن تتسبب الكائنات الحية الدقيقة، مثل البكتيريا الهوائية واللاهوائية، في سوائل الأشغال المعدنية القائمة على الماء في التآكل الناجم عن الميكروبات. تعمل البكتيريا الهوائية على تحلل الجزيئات طويلة السلسلة في مواد التشحيم، مكونةً الأحماض التي تسبب التآكل، بينما تنتج البكتيريا اللاهوائية مركبات الكبريت، مما يؤدي إلى تغير اللون.
التنفس البكتيري

4- التدابير المضادة للوقاية من التآكل
- عوامل التخميل
يمكن أن تشكل المعادن طبقة أكسيد طبيعية للتخميل، أو يمكن استخدام أملاح معينة لإنشاء طبقة واقية على سطح المعدن. على سبيل المثال، يمكن تخميل الحديد عن طريق الغمر في النيتريت أو الكرومات أو الموليبدات.
- الأفلام العضوية
يمكن تطبيق الأغشية العضوية، مثل الطلاءات ذات الأساس الزيتي، على الأسطح المعدنية، مما يشكل حاجزًا بين المعدن وبيئته. ومع ذلك، توفر هذه الطريقة حماية مؤقتة فقط.
- مثبطات البكتيريا
إذا كان التآكل ناتجًا عن البكتيريا، فيمكن استخدام مبيدات الجراثيم لتثبيط البكتيريا الهوائية، بينما يمكن إضافة الأكسجين للسيطرة على البكتيريا اللاهوائية. إذا كان التآكل الميكروبي واسع النطاق بالفعل، فقد يلزم استبدال سائل التشغيل لمنع المزيد من الضرر.

